Pasangan elektron yang
digunakan secara bersama pada pembentukan ikatan kovalen yang terletak
diantara dua inti atom akan ditarik oleh kedua inti atom yang
berikatan. Akibatnya akan mempengaruhi distribusi elektron di antara
kedua inti yang berikatan. Kemampuan menarik elektron kearah dirinya
tergantung pada keelektronegatifan masing-masing unsur yang berikatan.
Untuk molekul unsur, seperti H2, Cl2 dan N2
ikatan kovalen yang terbentuk seratus persen bersifat kovalen. Hal ini
disebabkan kedua inti atom memiliki kemampuan yang sama untuk menarik
elektron ke arah dirinya, sehingga elektron ikatan akan terdistribusi
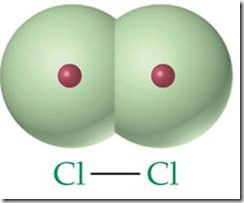
secara merata di antara kedua inti, seperti yang ditunjukan pada Gambar. Ikatan yang terbentuk dengan kemampuan menarik pasangan elektron yang sama kuat disebut ikatan kovalen nonpolar.
Gambar gambar Penyebaran elektron pada ikatan kovalen nonpolar Cl-Cl
Apabila kedua atom yang
berikatan berbeda misalnya pada HF, HCl dan HI, maka ikatan yang
terbentuk tidak sepenuhnya bersifat kovalen. Hal ini yang dinamakan
ikatan kovalen polar. Dikatakan ikatan kovalen polar karena kedua atom
yang berikatan terdapat gaya elektrostatik.
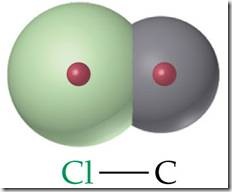
Gambar Ikatan kovalen polar C-Cl
Berdasarkan perbedaan kelektronegatifan, suatu ikatan kovalen dikatakan ikatan kovalen polar apabila suatu atom mampu menarik elektron ikatan ke arah dirinya tanpa melakukan perpindahan secara sempurna.
Semakin besar perbedaan
keelektronegatifan unsur-unsur yang berikatan, semakin polar ikatan
yang terbentuk bahkan mendekati sifat ionik. HX (X = Cl, Br, I, F), H2O, CO2, CCl4, BeCl2, BeCl3 dan NH3 merupakan beberapa contoh senyawa dengan ikatan kovalen polar. Misalnya
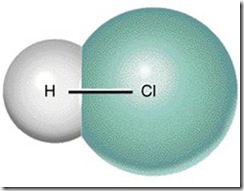
HCl, meskipun atom H dan Cl sama-sama menarik pasangan elektron ikatan,
tetapi keelektronegatifan Cl lebih besar dari atom H sehingga
distribusi elektron ikatan lebih terkonsentrasi pada Cl.
Gambar ikatan kovalen polar H-Cl
Molekul Polar dan Nonpolar
Suatu senyawa yang memiliki ikatan kovalen polar, belum tentu molekul yang dimiliki bersifat polar.
Demikian juga untuk ikatan kovalen nonpolar, molekul yang dimiliki
belum tentu bersifat nonpolar. Kepolaran suatu molekul dinyatakan
menggunakan suatu besaran yang disebut momen dipol (µ). Besarnya momen
dipol suatu molekul ditentukan menggunakan persamaan berikut.
µ = Q x r 1 D = 3,33 x 10-30 C.m (coulombmeter)
µ = 0 → molekul nonpolar
µ > 0 atau µ ≠ 0 → molekul polar
keterangan:
µ = momen dipol (D, debye)
Q = selisih muatan (Coulomb)
r = jarak antara muatan positif dengan muatan negatif (m)
Semakin besar harga
momen dipol, semakin polar senyawa yang bersangkutan bahkan mendekati
ke sifat ionik. Harga momen dipol beberapa molekul seperti yang tertera
pada Tabel.
|
molekul |
Momen dipol (D) |
molekul |
Momen dipol (D) |
|
NO NH3 HF HCl HBr HI H2O |
0,159 0,23 1,78 1,078 0,82 0,44 1,85 |
CO CO2 CHCl3 CH4 CCl4 BF3 BF2 |
0,112 0 1,09 0 0 0 0 |
Momen dipol merupakan suatu besaran vektor yang digambarkan menggunakan moment ikatan.
Jika jumlah vektor momen-momen ikatan lebih besar dari nol, maka
molekul tersebut bersifat polar, sebaliknya jika jumlah vektor
momen-momen ikatan sama dengan nol, maka maka molekul tersebut bersifat
nonpolar.
Momen ikatan terbentuk jika dua atom yang berikatan dalam suatu senyawa memiliki perbedaan keelektronegatifan.
Elektron yang yang ditarik oleh atom yang lebih elektronegatif
menunjukan arah momen ikatan dan ditunjukan menggunakan tanda → dari
atom yang kurang elektronegatif menuju atom yang lebih elektronegatif.
Akibat tarikan elektron
yang terjadi, terbentuk semacam kutub negatif pada atom yang lebih
elektronegatif, sedangkan pada atom yang kurang elektronegatif akan
terbentuk semacam kutub positif.
Kutub positif atau negatif yang terbentuk disebut muatan parsial,
yang digambarkan menggunakan simbol delta (δ). Muatan parsial negatif
(δ¯) diberikan pada unsur yang lebih elektronegatif dan muatan parsial
positif (δ+) diberikan pada unsur yang kurang elektronegatif (lebih elektropositif).
Berikut contoh menggambar muatan parsial pada molekul HCl.
Dari contoh di atas terlihat bahwa terdapat muatan positif dan negatif pada tanda δ yang digunakan.
Tanda tersebut tidak sama dengan +1 atau -1 seperti pada simbol ion,
tetapi tanda ini hanya menggambarkan elektron ikatan tidak sepenuhnya
dipindahkan ke atom Cl.
Untuk senyawa
diatom yang disusun oleh unsur yang sejenis, molekul yang dimiliki
selalu bersifat nonpolar kecuali ozon yang bersifa polar. Hal ini
disebabkan dua atom penyusun senyawa memiliki keelektronegatifan sama
sehingga tidak terbentuk momen ikatan. Sedangkan untuk senyawa diatom
yang disusun oleh dua atom yang berbeda molekul yang dimiliki selalu
bersifat polar karena adanya perbedaan keeltronegatifan.
Tetapi untuk senyawa-senyawa
yang tersusun lebih dari dua atom, kepolaran molekul tidak dapat
ditentukan jika hanya didasarkan pada perbedaan keelektronegatifan.
Hal ini disebabkan senyawa-senyawa tertentu walaupun memiliki ikatan
kovalen polar tetapi molekulnya bersifat nonpolar. Misalnya CCl4, CO2 dan BeCl2 merupakan beberapa senyawa dengan ikatan kovalen polar tetapi memiliki molekul yang nonpolar.
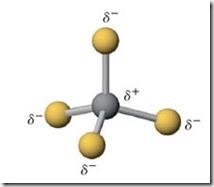
Pada molekul CCl4, yang mempunyai bentuk molekul tetrahedaral dengan C sebagai atom pusat dan dikelilingi oleh 4 atom Cl seperti pada Gambar.
Perbedaan keelektronegatifan C dan Cl adalah sebesar 3-2,5 = 0,5.
Jadi ikatan C–Cl termasuk ikatan kovalen (tepatnya ikatan kovalen
polar) karena perbedaan keeltronegatifan lebih kecil 1,7. Walaupun
ikatan C–Cl berupa ikatan kovalen polar tetapi molekulnya bersifat
nonpolar.
Hal ini disebabkan, bentuk tetrahedral dari molekul CCl4
dapat dikatakan simetrism karena memiliki pusat simetri pada atom C
ditengah, sehingga jumlah momen ikatan yang sama dengan nol. Atau dapat
dikatan tarikan elektron akibat adanya perbedaan keelektronegatifan
saling meniadakan atau saling menguatkan (perhatikan tanda panah pada
strutur).
Hal ini dapat diandaikan, suatu benda yang berada di tengah-tengah
ditarik dari empat sudut dengan kekuatan sama, maka benda tersebut
tidak akan bergerak. Karena hal inilah molekul CCl4 bersifat nonpolar.
Jika CCl4
salah satu atom Cl diganti oleh atom lain misalnya H, maka sifat
molekul yang awalnya nonpolar berubah menjadi polar. Hal ini disebabkan
kepolaran ikatan C-H berbeda dengan kepolaran ikatan C-Cl, sehingga
momen dipol yang terbentuk tidak saling meniadakan. Tetapi apabila
semua atom C diganti oleh atom H maka molekulnya bersifat nonpolar
karena kepolaran semua ikatan C–H sama besar sehingga mpmen ikatan yang
terbentuk saling meniadakan.
Pada molekul BCl2 dan CO2 mempunyai bentuk molekul linear dengan B dan C sebagai atom pusat.
Atom Cl dan atom O lebih
elektronegatif dibanding atom B dan C yang bertindak sebagai atom pusat
(pada gambar yang berwarna hitam), sehingga elektron ikatan lebih
tertarik kearah atom Cl dan O. Namun, atom B dan C masing-masing
mengikat 2 atom yang sejenis maka momen ikatan yang terbentuk tertarik
ke arah yang berlawanan dengan kekuatan yang sama, sehingga molekulnya
bersifat nonpolar.
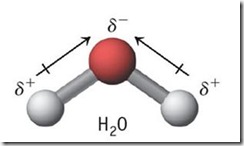
Molekul H2O walaupun rumus molekulnya mirip dengan CO2 dan BCl2 tetapi bersifat polar.
Hal ini disebabkan, pada molekul H2O, atom O sebagai atom pusat masih memiliki pasangan elektron bebas. Hal ini menyebabkan molekul H2O tidak berbentuk linear seperti molekul CO2 dan BCl2, sehingga momen ikatan yang terbentuk tidak saling menguatkan atau tidak saling meniadakan.


Tidak ada komentar:
Posting Komentar